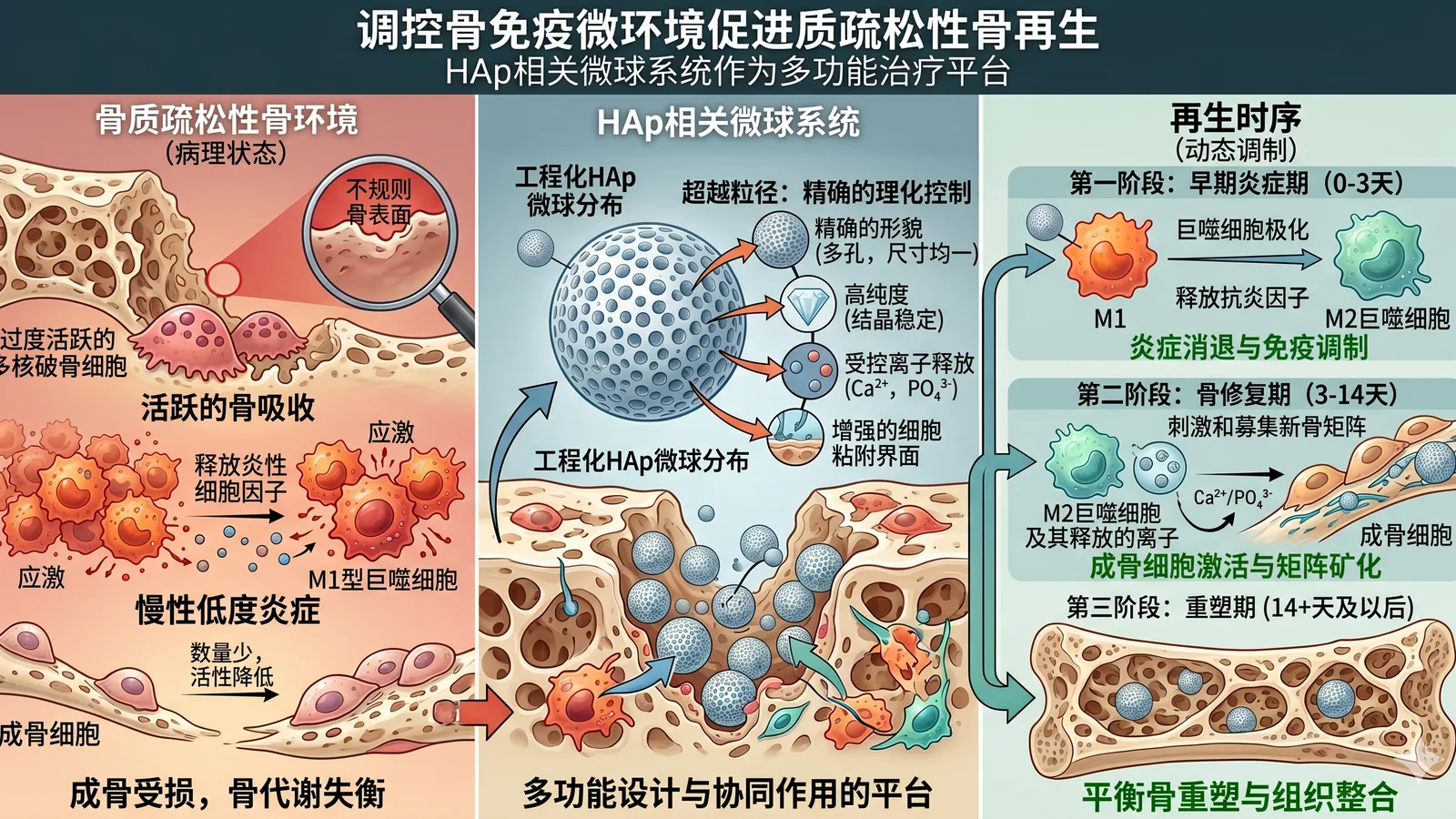
骨质疏松性骨缺损的修复,面临的挑战远超骨组织结构缺失本身——骨代谢失衡、慢性低度炎症持续、骨吸收增强以及局部再生能力下降,共同构成了复杂的微环境异常。近年的研究显示,单纯依赖“填充”和“骨传导”的材料设计思路已显不足,骨免疫微环境、骨吸收—骨形成平衡以及组织整合过程的协同调控,开始成为核心议题。
在这一背景下,羟基磷灰石(Hydroxyapatite, HAp)相关材料的研究视角也在发生变化:除了传统意义上的被动支撑角色,研究者正越来越多地关注其在骨修复微环境调节中的主动参与潜力。结合近期关于 HAp 与工程化微球体系的研究进展,本文梳理 HAp 相关微球在形貌设计、理化性质控制及微环境调节方面的潜在意义,并讨论其对骨修复材料开发的启示。
骨质疏松性骨缺损修复为何更具挑战
与一般骨缺损相比,骨质疏松性骨缺损的复杂性并不只来自“缺了一块骨”,而在于其所处的是一个已经失衡的病理微环境。近期综述指出,骨质疏松相关缺损往往伴随着骨吸收活跃、成骨能力下降、炎症信号持续以及局部微环境支持不足等多重问题,因此传统仅依赖物理支撑或单一机制干预的策略,往往难以充分应对这类复杂场景。
围绕这一认识,越来越多研究开始从“重建骨微环境”而不仅是“填补缺损”的角度来设计新型骨修复材料。从材料研发的角度看,这意味着评价标准也在变化。一个材料是否具备潜力,不再只取决于其是否具有基本骨传导性,而更取决于它能否在骨修复早期与宿主反应形成积极交互,能否在后续过程中支持骨形成、抑制异常骨吸收,并维持局部修复环境的相对稳定。
HAp 的研究视角正在发生变化
HAp 长期以来是骨修复领域的经典材料,最常被强调的是其良好的生物相容性、与骨组织成分的相似性以及骨传导能力。近期针对 2015–2025 年体内研究的系统综述版本显示,HAp 在骨重塑、骨再生和骨替代中的应用仍然非常活跃,而研究重点也在逐渐深入——相比“是否能填充和支撑”这一基础问题,当前更多讨论聚焦于组成、纯度、孔隙结构、表面性质和形貌参数如何影响体内修复反应。
这类变化与骨免疫研究的发展密切相关。当前越来越多研究将骨修复理解为一个涉及免疫反应、炎症消退、细胞募集、基质沉积和骨重塑连续发生的动态过程。在这一框架下,HAp 作为“被动骨样材料”的传统认知正在被拓展:其表面化学特征、离子环境、形貌结构及界面特性,均可能在修复早期的宿主反应调节中发挥作用。
对材料企业而言,这一变化也意味着:评价 HAp 微球时,关注点不应停留在“是不是 HAp”这一表层问题,而应进一步落到材料特征是否稳定、可设计、可重复。
为什么“微球”与“相关微球体系”值得关注
在不规则骨缺损修复中,微球体系的一个突出优势,在于其更容易适配复杂缺损空间,并可作为复合体系、注射体系或打印体系中的功能单元参与材料设计。与部分传统块状支架相比,微球通常在装载活性组分、调节界面接触、构建可组合配方以及提升加工灵活性方面更具工程化潜力。
对于骨质疏松性缺损这类病理环境复杂的场景,微球作为“平台”而非单一颗粒材料来理解,往往更符合当前研究方向。需要注意的是,当前关于“时序性调控骨免疫微环境”的较直接证据,更多来自工程化复合微球体系研究,而不完全等同于“单一 HAp 微球本体已完成全部机制验证”。
2026 年发表于 Journal of Orthopaedic Translation 的研究展示了多功能微球体系如何通过分阶段干预炎症、氧化应激与骨重塑平衡,促进骨质疏松性骨缺损修复。需要指出的是,该研究并非 HAp 微球本体研究,而是为“微球平台如何参与骨免疫时序调控”提供了可参考的工程化思路。
对 HAp 相关微球材料开发的启示:关键不止粒径
在实际开发中,粒径当然重要,但并不是唯一决定因素。近期关于 HAp 体内研究的系统综述和骨质疏松骨微环境综述都提示,材料的纯度、粒径分布、孔隙结构、表面特征、结晶状态以及批次间一致性,都会影响其在体内的界面行为和后续修复表现。
对于上游材料供应端而言,这些参数不仅关乎实验数据的稳定性,也直接影响下游器械、复合支架和生物制造体系的可开发性。以 HAp 相关微球为例,较窄的粒径分布通常有助于提升加工一致性与体系均匀性;稳定的纯度控制有助于减少杂质带来的不确定影响;而合理设计的表面和孔隙结构,则更有利于材料与细胞、组织液和基质环境形成有效接触。
需要强调的是,这些特征本身并不自动等于“更好的临床结果”,但它们构成了高质量下游研发的重要基础。对于 3D 打印生物墨水、复合缓释载体、注射型填充体系或多相支架而言,这类底层材料一致性往往决定了产品开发的上限。
从研究趋势到产业转化:HAp 相关微球的现实意义
从当前研究趋势看,骨修复材料的竞争焦点已不止于“单一材料是否有效”,“材料能否在复杂微环境中发挥协同作用”成为新的关键命题。与之对应,越来越多研究将离子释放、免疫调节、抗炎、抗氧化、成骨支持和基质模拟纳入同一设计框架,而不是只围绕单一骨传导性展开讨论。
对 HAp 相关微球来说,这一趋势意味着其更适合作为复合材料平台、功能添加单元或界面优化模块去参与下一代骨修复体系开发,而不是仅作为传统意义上的惰性颗粒存在。同时也应看到,现阶段这一领域的高质量证据仍以材料研究、动物实验和机制探索为主,距离广泛临床转化仍需要更系统的标准化评价与长期验证。
在骨免疫调控与微环境重塑成为重要研究方向的背景下,高品质 HAp 相关微球可作为骨修复复合体系与组织工程支架开发中的材料基础之一,为后续配方设计、界面优化和标准化评价提供更稳定的上游支撑。
结语
骨质疏松性骨缺损的修复,本质上是一个“重建结构”与“重塑微环境”并行推进的过程。随着骨免疫与组织工程研究不断深入,HAp 的研究价值也随之延伸至更强调界面交互和系统设计的功能材料维度,而非仅停留在传统骨传导层面。
对 HAp 相关微球而言,真正值得关注的,不只是其作为颗粒材料的存在形式,更是其能否在高纯度、可控形貌、稳定一致性和复合体系适配性之间建立可靠平衡。未来,围绕这类材料的讨论重点也会发生变化:从“有没有”,逐渐转向“能否被更精准地设计、评价和转化”。
参考研究
- Fendi F, et al. In vivo studies of hydroxyapatite for bone remodeling, regeneration, and replacement: A bibliometric analysis (2015–2025) and systematic review. F1000Research. 2026;15:543. DOI: 10.12688/f1000research.178985.1.
- Lu X, Zhang A, Zhang C, et al. Targeting the osteoporotic bone microenvironment: Mechanistic insight and therapeutic biomaterials for accelerating bone regeneration. Bioactive Materials. 2026;62:96–122. DOI: 10.1016/j.bioactmat.2026.02.024.
- Luo Z, Ma J, Yang Y, et al. Engineering multifunctional microspheres for sequential regulation of osteoimmune microenvironment and bone remodeling balance to promote regeneration of osteoporotic bone defects. Journal of Orthopaedic Translation. 2026;57:101054. DOI: 10.1016/j.jot.2026.101054.